氢氧燃料电池以氢气作燃料、氧气作氧化剂通过燃料的燃烧反应,将化学能转变为电能的一类燃料电池。氢氧从外部通过管道输入电池进行电化学反应并输出电能。具有转换效率高、容量大、比能量高、功率范围广、不用充电等优点。
氢氧燃料电池按电池结构和工作方式分为离子膜、培根型和石棉膜三类。
1.离子膜氢氧燃料电池:用阳离子交换膜作电解质的酸性燃料电池,现代采用全氟磺酸膜。电池放电时,在氧电极处生成水,通过灯芯将水吸出。这种电池在常温下工作、结构紧凑、重量轻,但离子交换膜内阻较大,放电电流密度小。
2.培根型燃料电池:属碱性电池。氢、氧电极都是双层多孔镍电极(内外层孔径不同),加铂作催化剂。电解质为80%~85%的苛性钾溶液,室温下是固体,在电池工作温度(204~260°C)下为液体。这种电池能量利用率较高,但自耗电大,起动和停机需较长的时间(起动需24小时,停机17小时)。
3.石棉膜燃料电池:也属碱性电池。氢电极由多孔镍片加铂、钯催化剂制成,氧电极是多孔银极片,两电极夹有含35%苛性钾溶液的石棉膜,再以有槽镍片紧压在两极板上作为集流器,构成气室,封装成单体电池。放电时在氢电极一边生成水,可以用循环氢的办法排出,亦可用静态排水法。这种电池的起动时间仅15分钟,并可瞬时停机。 比磷酸铁锂电池要更环保。
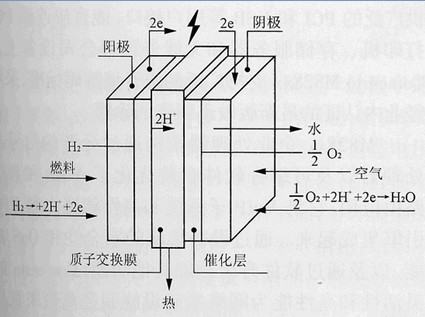
工作时向负极供给燃料(氢),向正极供给氧化剂(氧气)。氢在负极上的催化剂的作用下分解成正离子H+和电子e-。氢离子进入电解液中,而电子则沿外部电路移向正极。用电的负载就接在外部电路中。在正极上,氧气同电解液中的氢离子吸收抵达正极上的电子形成水。这正是水的电解反应的逆过程。
1、材料价廉
2、操作简单
3、安全
4、高效
5、无污染
氢氧燃料电池(中性介质):
正极:O2 + 2H2O + 4e- → 4OH-
负极:2H2 - 4e- → 4H+
总反应式:2H2 + O2 == 2H2O
氢氧燃料电池(酸性介质):
正极:O2 + 4H+ + 4e- → 2H2O
负极:2H2 - 4e-→ 4H+
总反应式:2H2 + O2 == 2H2O
氢氧燃料电池(碱性介质):
正极:O2 + 2H2O + 4e- → 4OH-
负极:2H2 - 4e- + 4OH- → 4H2O
总反应式:2H2 + O2 == 2H2O
维库电子通,电子知识,一查百通!
已收录词条45417个